Contents
【問題】
【難易度】★★☆☆☆(やや易しい)
\[
\begin{eqnarray}
\end{eqnarray}
\]
\( \ \boxed { 19\strut } \ \)の中に入れるべき最も適切な字句等をそれぞれの解答群から選び、その記号を答えよ。
(16) 電気化学システムは、基本的には電解質、それをはさむ二つの電極及び外部回路からなっている。電極と電解質の間で電子の受け渡しが行われ、電解質は\( \ \boxed { 19\strut } \ \)伝導体としての役割を担う。
<\( \ \boxed { 19\strut } \ \)の解答群>
\[
\begin{eqnarray}
&ア& イオン &イ& 電子 &ウ& 熱 \\[ 5pt ]
\end{eqnarray}
\]
【ワンポイント解説】
電気化学に関する知識問題です。熱分野を受験される方は、答えだけ暗記しても問題ありません。一方、電気分野を受験される方に取って、課目\( \mathrm {Ⅳ}\)電気化学の基礎となる問題です。電気化学を選択される方は、化学反応式からどのようなことが起きるのか、アノードやカソードなどの意味を理解する必要があります。他の過去問と組み合わせて、繰り返し演習していくようにしていきましょう。
1.電気化学システムの構造
構造は問題文と図1のように、2つの電極と外部回路と電解質から成り立っています。
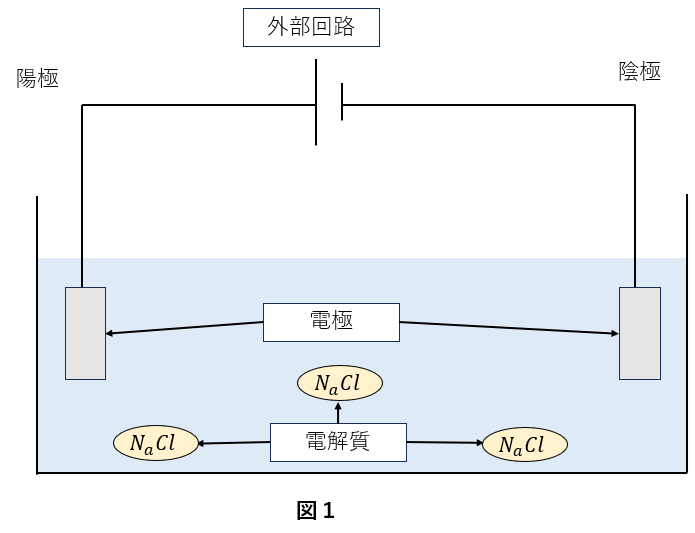
小学生の頃の理科で、「純水は電気が流れないが、食塩を混ぜると電気が流れる」という実験をされた方もいらっしゃると思います。これは、電解質である食塩がイオン伝導体として、電極で電子やイオンのやり取りをしているから、電気が流れるということです。
2.電気化学の流れ
電気化学の一連の流れを、食塩の電気分解を例に図2で表しています。
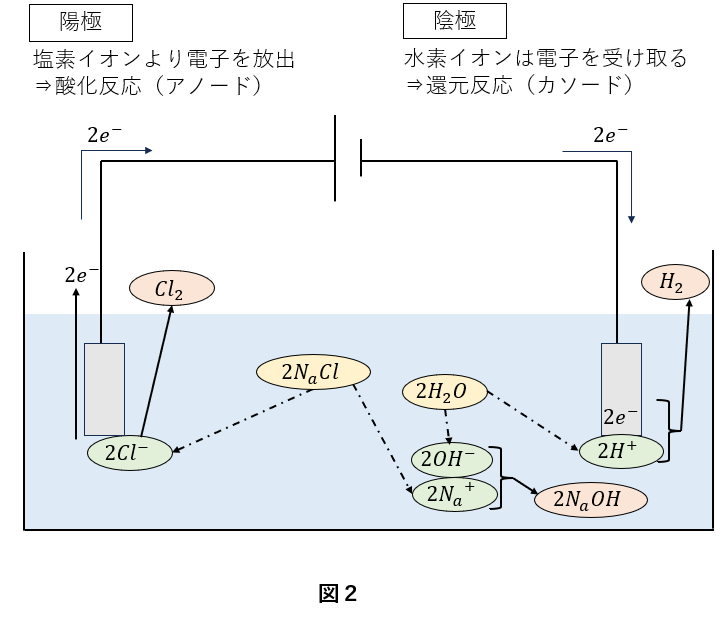
化学反応式は以下のようになります。
\[
\begin{array}{llcl}
\mathrm{陽極:} & \mathrm{2Cl^-} \rightarrow \mathrm{Cl_2} + \mathrm{2e^-} \\[ 5pt ]
\mathrm{陰極:} & \mathrm{2Na^+} + \mathrm{2H^+} + \mathrm{2OH^+} + \mathrm{2e^-} \rightarrow \mathrm{H_2} + \mathrm{2NaOH} \\[ 5pt ]
\mathrm{全体:} & \mathrm{2NaCl} + \mathrm{2H_2O} \rightarrow \mathrm{Cl_2} + \mathrm{2H_2} + \mathrm{2NaOH} \\[ 5pt ]
\end{array}
\]
化学反応式自体は覚えなくても問題ないですが、各極で酸化と還元どちらの反応が起こっているか、どちらがアノードかカソードかは、覚えておきましょう。
※この方法は水酸化ナトリウム製造に応用されていますが、実際はイオン交換膜などを使用します。
【解答】
(19)解答:ア
ワンポイント解説1の通り、電解質はイオン伝導体としての役割を担っています。
















